Ecuación para bases débiles
[BH+]=√F⋅Kb[BH+]=√F⋅Kb
Tags | |
UUID | 6f679532-55ec-11e7-9770-bc764e2038f2 |
La ecuación para la base débil calcula la concentración desconocida de la base débil disociada en una solución en una solución.
La reacción de base débil común es
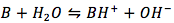
para la cual la ecuación de equilibrio es
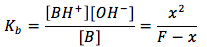
ya que normalmente se nos da la concentración formal, el [BH+]=x es desconocido y debemos resolverlo.En primer lugar suponemos que 'x' va a ser mucho menor que la concnetración formal, por lo que la ecuación de equilibrio se convierte en
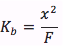
Multiplicando ambos lados por la concentración formal que obtenemos
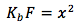
tomando una raíz cuadrada de ambos lados obtenemos
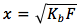
Descripción
La ecuación es
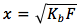
dónde
- Kb es la constante de equilibrio de base
- F es la concentración formal en unidades de (mol/L)
- x es la concentración de la base disociada [BH+] en unidades de (mol/L)
Referencias
Harris, 9th Edition. Pp.195
- Comments
- Attachments
- Stats
No comments |
This site uses cookies to give you the best, most relevant experience. By continuing to browse the site you are agreeing to our use of cookies.
