Calculadora Para La Ley de Boyle
Tags | |
UUID | 952b9f4f-3a8f-11e7-9770-bc764e2038f2 |
La calculadora de la Ley de Boyle calcula las presiónes y volumes iniciales y finales basados en las ecuaciónes de la Ley de Boyle: P1 • V1 = P2 • V2, donde P1 es la presión inicial, V1 es el volumen inicial, P2 es la presión final y V2 es el volumen final de una cantidad fija de gas a una temperatura constante. La calculadora maneja automáticamente numerosas unidades de presión y volumen. Haga clic en uno de los siguientes parámetros:
- (P1) Para calcular la presión inicial con la Ley de Boyle, haz click aquí.
- (V1) Para calcular el volumen inicial con la Ley de Boyle, haz click aquí.
- (P2) Para calcular la presión final con la Ley de Boyle, haz click aquí.
- (V2) Para calcular el volumen final con la Ley de Boyle, haz click aquí.
La Ley de Boyle es una ley experimental que describe cómo la presión de un gas tiende a disminuir a medida que aumenta el volumen de un gas.
Artículos Relacionados:
- La Ley de Charles enseña la relación entre la temperatura y el volumen. Para calcular con la Ley de Charles, haz click aquí. V1V1•T2T2 = V2V2•T1T1
- La Ley de Gas Combinada enseña la relación entre la temperatura, el volumen, y la presión. Para calcular con la Ley de Gas Combinada, haz click aquí. P•V / T = k
- La Ley de Gay-Lussac enseña la relación entre la temperatura y la presión. Para calcular con la Ley de Gay-Lussac, haz click aquí. T1T1•P2P2=T2T2•P1P1
- La Ley de Gas Ideal enseña la relación entre la presión, el volumen, el número de moles, y la temperatura. Para calcular con la Ley de Gas Ideal, haz click aquí. P•V = n•R•T
Acerca de la Ley de Boyle
La Ley de Boyle establece que el volumen de un gas varía inversamente con su presíon si la temperatura se mantiene constante. La Ley de Boyle describe la relación de un gas ideal dónde la masa y la temperatura se mantienen constantes. En estas condiciones, el volumen del gas variará inversamente con la presión absoluta. Una reafirmación de la Ley de Boyle es:
La presión absoluta ejercida por una masa dada de un gas ideal es inversamente proporcional al volumen que ocupa si la temperatura y la cantidad de gas permanecen inalteradas dentro de un sistema cerrado.
Haz clic en el enlace La Ley de Boyle (la presión final) para más información.
Uso
Cada uno de las cuatro ecuaciónes de esta calculadora se deriva de la simple relación de la ley de Boyle: P1⋅V1=P2⋅V2P1⋅V1=P2⋅V2. Cada ecuación supone una temperatura fija y una cantidad fija de gas.
Especificamente:
- La Ley de Boyle (la presión final); Puedes usar esta ecuación para calcular la presión final (P2) cuando tienes un cambio en el volumen (V2 - V1) y la presión inicial (P1).
- La Ley de Boyle (la presión inicial); Puedes usar esta ecuación cuando tienes un cambio en el volumen (inicial y final; V2 - V1) con la final presión (P2).
- La Ley de Boyle (el volumen final); Puedes usar esta ecuación para calcular la volumen final (V2) cuando tienes un cambio en la presión (P2 - P1) y tienes la volumen inicial (V1).
- La Ley de Boyle (el volumen inicial); Puedes usar esta ecuación cuando tienes la volumen inicial (V1 ) del gas antes de un cambio en la presión (P2 - P1) y con la volumen final (V2)
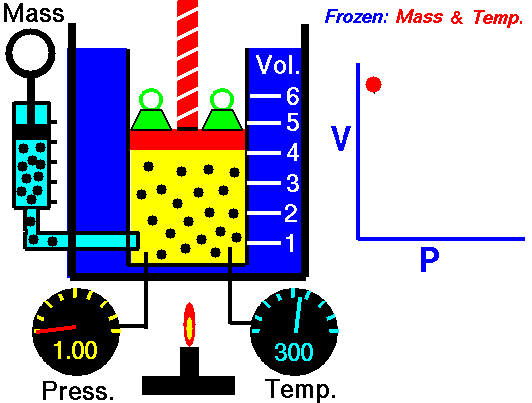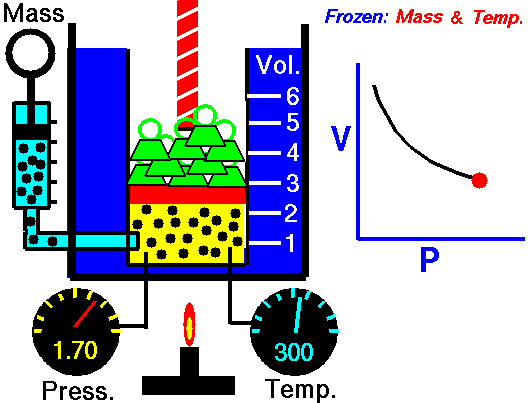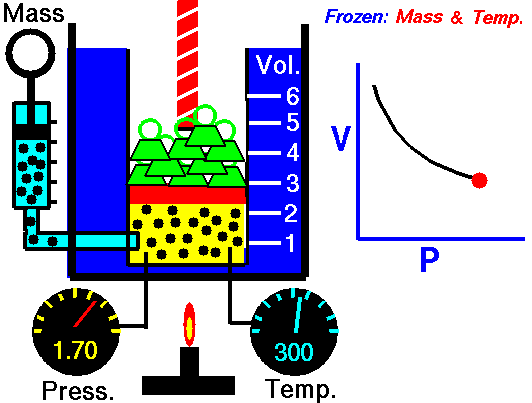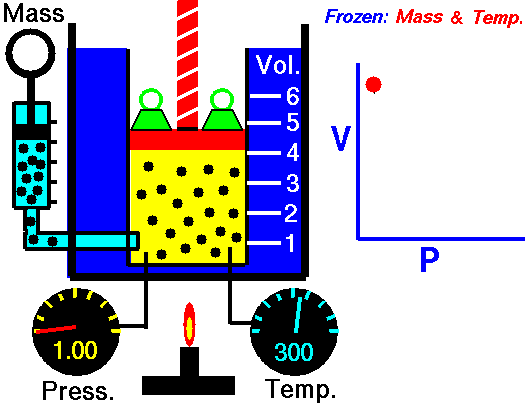 pressure is inversely proportional to volume
pressure is inversely proportional to volume
Solicitud
Existen diferente maneras de calcular la presión y el volumen antes y después del cambio en el volumen o la presión (NOTA: La masa y temperatura del gas se deben mantener constante).
La ley de Boyle sigue las reglas generales de los gases ideaes. La mayoría de los gases se comportan como gases ideales a presiones y temperaturas moderadas. Sin embargo, a medida que la tecnología permitieron presiones más altas y temperaturas más bajas a ser examinadas, se identificaron desviaciones del comportamiento del gas ideal. Posteriormente se determinó que la relación entre la presión y el volumen sólo se puede describir con preción y el volumen sólo se puede describir con precisión empleando la teoría del gas real.
Más Información
Equations and Data Items
- Comments
- Attachments
- Stats
No comments |
