La Ley de Velocidad Primero Orden (forma integral)
Tags | |
UUID | 15b8d8a6-55e2-11e7-9770-bc764e2038f2 |
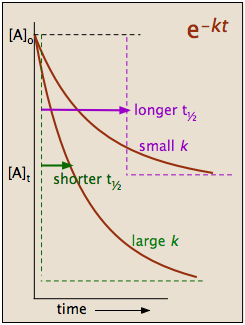
La ecuación para la ley de velocidad primero orden (forma integral)[1] calcula la velocidad en que los reactivos convierten a productos. A diferencia de la forma diferencial de la ecuación primero orden, la forma integral toma en cuenta la cantidad de reactivos ha estado convertir a productos en un punto específico en la reacción. Puedes encontrar una ecuación de integración completo aquí.
Descripción
La ecuación es
[A]=[A]oe−kt [2]
Donde
- [A]o representa la concentración inicial en las unidades de (mol/L)
- k representa el constante de velocidad en las unidades de (1/segundo)
- t representa el tiempo de la concentración en las unidades de (segundos)
Related Topics
Más Información
- Khan Academy: Rate law and reaction order
Referencias Bibliográficas
[1] https://en.wikipedia.org/wiki/Rate_equation
[2]Whitten, et al. 10th Edition. Pp. 626,629,631
[Picture]http://chemwiki.ucdavis.edu/Core/Physical_Chemistry/Kinetics/Reaction_Rates/First-Order_Reactions
This equation, La Ley de Velocidad Primero Orden (forma integral), is used in 1 page
Calculators
- Comments
- Attachments
- Stats
No comments |
This site uses cookies to give you the best, most relevant experience. By continuing to browse the site you are agreeing to our use of cookies.
