La Ley de Henry
Tags | |
UUID | 70604484-4d13-11e7-9770-bc764e2038f2 |
La ecuación de la Ley de Henry calcula la relación entre la presión[4] y la solubilidad del gas[5] en líquido[6]. Un químico de Inglaterra William Henry (1774-1836)[3] lo descubrió. La concentración del gas disuelto en disolvente[7] generalmente se calcula para un gas disuelto en agua en 20ºC (293.15K). La ecuación se derivó de una observación que la solubilidad de los gases aumentará si la presión parcial de las moléculas del gas por encima de la solución también aumenta. En resumen, la lay establece que en el equilibrio la cantidad de moléculas de gas disueltas en un volumen de líquido es directamente proporcional a la presión parcial que está en contacto con el líquido.
Descripción
La Ley de Henry se calcula de la siguiente manera:
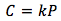 [2]
[2]
Donde :
- C representa la concentración del gas que se disuelve en el líquido en las unidades de (mol/L)
- k representa el constante de la ley de Henry en las unidades de (mol/L * atm)
- P representa la presión parcial de un gas en las unidades de (atm)
Puedes encontrar una lista amplia de constantes de la Ley de Henry en ingles aquí.[8]
*Nota: los gases que son solubles en agua no obedecen la Ley de Henry.
Otras Calculadoras
Temas relacionades
- Khan Academy: Henry's Law
- Crash Course: Partial Pressures & Vapor Pressure
- Henry's Law: Relationship Between Pressure and Solubility of a Gas
Referencias Bibliográficas
[1]Henry's law. (n.d.).
Retrieved May 26, 2016, from https://en.wikipedia.org/wiki/Henry's_law
[2] Whitten, et al. 10th Edition. Pp.514
[3]William Henry (chemist). (n.d.).
Retrieved May 26, 2016, from https://en.wikipedia.org/wiki/William_Henry_(chemist)
[4]Pressure. (n.d.). Retrieved May 26, 2016, from https://en.wikipedia.org/wiki/Pressure
[5]Gas. (n.d.). Retrieved May 26, 2016, from https://en.wikipedia.org/wiki/Gas
[6]Liquid. (n.d.). Retrieved May 26, 2016, from https://en.wikipedia.org/wiki/Liquid
[7]Solvent. (n.d.). Retrieved May 26, 2016, from https://en.wikipedia.org/wiki/Solvent
- Comments
- Attachments
- Stats
No comments |
