Calculadora para encontrar pOH con pH y pKw
Tags | |
UUID | ab81f96d-4baf-11e7-9770-bc764e2038f2 |
pOH[1] es la medición de la base de una solución. La medición de pOH se deriva de la medida de concentración de iones de hidróxido. Puesto que la concentración de iones es pequeña en la solución, se convierte mediante la ecuación anterior en pOH (la ecuación anterior es una derivación de una ecuación que puedes encontrar aquí) y se compara con una escala. La escala de pH oscila de 0 a 14, 0 siendo ácido y 14 siendo básico. En 25°C la concentración de cada ion (H+ and OH-) es 1.0x10-7 (mol/L), cuando ambas concentraciones permanecen iguales, entonces la solución se convierte en neutro, que es un pH de 7 en la escala.
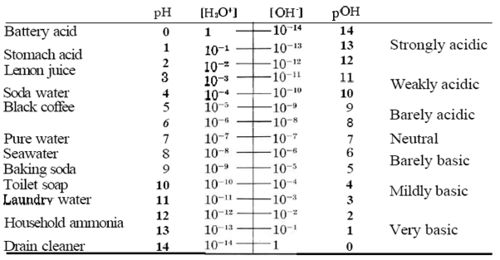
Descripción
La ecuación es
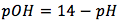 [2]
[2]
dónde:
- pH representa la medida de acidez (no tiene unidades)
- pOH representa la medida de la basicidad (no tiene unidades)
- pKw representa el logaritmo natural de el constante de equilibrio del agua, siempre es 14 (para más información acerca de pKw ir aquí)
Calculadoras Para Encontrar pH y pOH
- Calculadora para encontrar pH de [OH-]
- Calculadora para encontrar pH de [H+]
- Calculadora para encontrar pH con pOH y pKw
- Calculadora para encontrar pOH de [OH-]
- Calculadora para encontrar pOH de [H+]
- Calculadora para encontrar pOH con pH y pKw
Más Información
Referencias Bibliográficas
[1]https://es.wikipedia.org/wiki/POH
[2]Whitten, et al. 10th Edition. Pp.713
[pH diagram]http://wiki.chemprime.chemeddl.org/index.php/PH_and_pOH_in_Everyday_Life
Calculators
- Comments
- Attachments
- Stats
No comments |
