La Ley de Velocidad (Media Vidas)
La media vida de una reacción química se define como el tiempo necesario para que la mitad de la cantidad de una reacción se puede convertir en producto. Para encontrar las media vidas de diferente reacciónes, nosotros usamos las leyes de velocidad integral y las constantes de velocidad para relacionar concentración a tiempo. Hay tres diferente leyes de velocidad que se pueden usar para encontrar la media vida de una reacción química: orden cero, primero orden, segundo orden.
Orden Cero
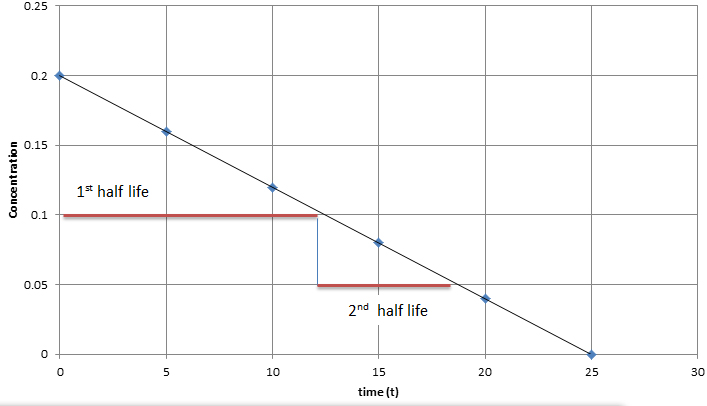
Para cinéticas orden cero, la media vida no es dependiente en la concentración de la sustancia. Dicho de otro modo, velocidad = k. Este se significa que no importa la cantidad de sustrato se añade, y no importa la cantidad de concentración presente en solución, la velocidad de la reacción no va aumentar. Una representación gráfica de este enseñaría datos lineal con una inclinación negativa, como se muestra en la imagen abajo. La ley de velocidad para una reacción orden cero es [A] = [A]0 - kt. Para encontrar la media vida para una reacción orden cero, se usa la ecuación t1/2 = [A]0 / 2k.
- k representa la constante temperatura-dependiente de la velocidad de reacción
- t1/2 representa la media vida
- [A]0 representa la concentración inicial
Primero Orden
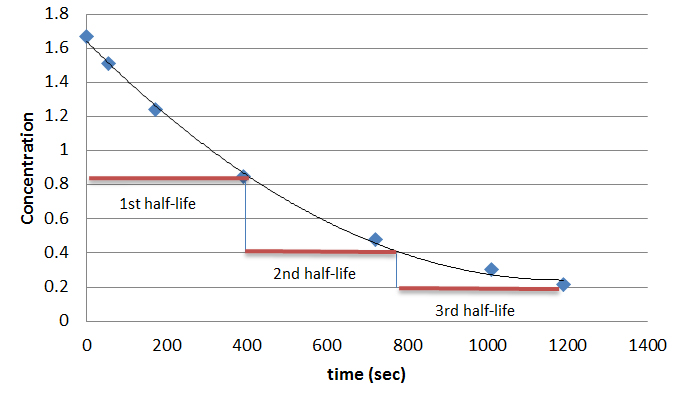
Reacciónes primero orden son dependiente en concentración; esta significa que si más sustrato es añadido, lo más rápido la reacción va proseguir. La velocidad para este orden es rate = k[A]. Reacciónes de primero orden tienen gráficos único, un ejemplo es el gráfico abajo. Nota como toma el mismo cantidad de tiempo para la concentración a disminuir entre puntos. La ley de velocidad para una reacción primero orden es [A] = [A]0e-kt. Se usa la ecuación t1/2 = 0.693 / k para encontrar la media vida para una reacción primero orden.
Donde
- k representa la constante temperatura-dependiente de la velocidad de reacción
- t1/2 representa la media vida
Segundo Orden
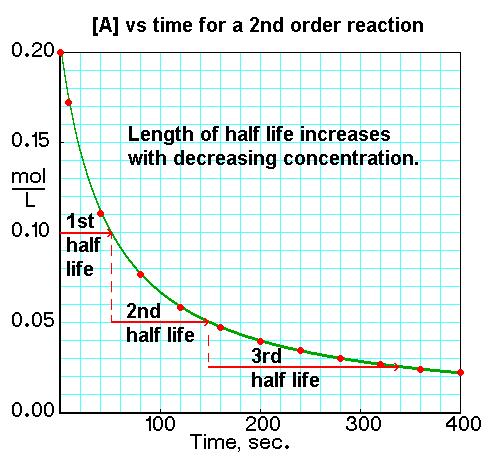
Reacciónes segundo orden son dependiente de concentración, igual que reacciónes primero orden; pero, reacciónes segundo orden reaccionan más rápido que reacciónes primero orden. La velocidad para reacciónes segundo orden es rate = k[A]2, así que la velocidad disminuye exponencialmente, a diferencia de reacciónes primero orden. La ley de velocidad es 1/[A] = kt + 1/[A]0 y la ecuación que se usa para encontrar la media vida de una reacción segundo orden es t1/2 = 1 / k[A]0.
Donde
- k representa la constante temperatura-dependiente de la velocidad de reacción
- t1/2 representa la media vida
- [A]0 representa la concentración inicial
Referencias Bibliográficas
Whitten, et al. "Chemistry" 10th Edition. Pp. 626-631
Equations and Data Items
- Comments
- Attachments
- Stats
No comments |